Grafite, formula molecolare: C, peso molecolare: 12.01, è una forma di elemento carbonio, ciascun atomo di carbonio è collegato da altri tre atomi di carbonio (disposti in esagoni a nido d'ape) per formare una molecola covalente. Poiché ogni atomo di carbonio emette un elettrone, quelli che possono muoversi liberamente, quindi la grafite è un conduttore.
La grafite è uno dei minerali più morbidi e i suoi usi includono la realizzazione di mine e lubrificanti per matite. Il carbonio è un elemento non metallico situato nel gruppo IVA del secondo ciclo della tavola periodica. La grafite si forma ad alte temperature.
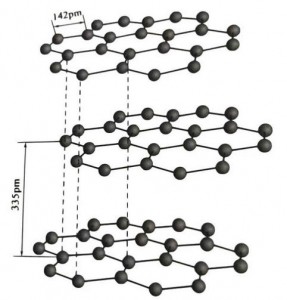
La grafite è un minerale cristallino di elementi di carbonio e il suo reticolo cristallino è una struttura a strati esagonali. La distanza tra ciascuno strato di rete è 3,35 A e la spaziatura degli atomi di carbonio nello stesso strato di rete è 1,42 A. È un sistema cristallino esagonale con una scissione a strati completa. La superficie di scissione è costituita principalmente da legami molecolari, meno attraenti per le molecole, quindi il suo galleggiamento naturale è molto buono.
Nei cristalli di grafite, gli atomi di carbonio nello stesso strato formano un legame covalente con ibridazione sp2 e ciascun atomo di carbonio è collegato ad altri tre atomi in tre legami covalenti. I sei atomi di carbonio formano un anello a sei continui sullo stesso piano, che si estende in una struttura a lamelle, dove la lunghezza del legame CC è 142 µm, che è esattamente all'interno dell'intervallo di lunghezze del legame del cristallo atomico, quindi per lo stesso strato , è un cristallo atomico. Gli atomi di carbonio sullo stesso piano hanno un'orbita p, che si sovrappone all'altra. Gli elettroni sono relativamente liberi, equivalenti agli elettroni liberi nei metalli, quindi la grafite può condurre calore ed elettricità, che è la caratteristica dei cristalli metallici. Quindi classificati anche come cristalli metallici.
Lo strato intermedio di cristallo di grafite è separato da 335pm e la distanza è ampia. È combinato con la forza di van der Waals, cioè lo strato appartiene al cristallo molecolare. Tuttavia, poiché il legame degli atomi di carbonio nello stesso strato piano è molto forte ed estremamente difficile da distruggere, anche il punto di dissoluzione della grafite è molto elevato e le sue proprietà chimiche sono stabili.
In considerazione della sua speciale modalità di legame, non può essere considerata un cristallo singolo o un policristallo, la grafite è ora generalmente considerata un cristallo misto.
Orario di pubblicazione: 31 luglio 2023